早在20世紀, Alois Alzheimer 首先描述了50歲女性中進行性記憶喪失和混亂的疾病。 在她去世後,他檢查了她的大腦,發現它充滿了不尋常的蛋白質塊,稱為斑塊。 一個多世紀後,我們知道這些斑塊中充滿了一種叫做β-澱粉樣蛋白的蛋白質,並且是這種疾病的標誌,具有阿爾茨海默氏症的名字。 雖然已發現阿爾茨海默病的其他特徵,但β-澱粉樣蛋白是導致這種無法治癒的疾病的主要原因的理論占主導地位。
“β-澱粉樣蛋白假說”有許多微妙的變化,但一般來說理論認為β-澱粉樣蛋白在大腦中積累,然後聚集在一起。 在這個過程的某個地方,大腦中的神經細胞受到損傷,導致記憶喪失和阿爾茨海默病的其他症狀。 所以治療這個的方法應該是相當簡單的:停止結塊,你將停止疾病。
不幸的是,數十年的研究,數百萬美元的投資和許多後來的失敗的臨床試驗,似乎這種方法不起作用。 最近發生令人失望的結果的斑塊破壞治療是aducanumab--一種基於抗體的療法,旨在堅持並破壞β-澱粉樣蛋白。
初步數據表明,治療確實可以清除大腦中的β-澱粉樣蛋白。 但本週,Biogen和Esai,aducanumab背後的製藥公司, 結束臨床試驗 早期涉及數千名患者, 說明 “試驗在完成時不太可能滿足其主要終點”。
這導致許多人質疑是否應該放棄阿爾茨海默病的澱粉樣蛋白假說。 實際上,很少有神經科學家仍然認為β-澱粉樣斑塊本身會導致阿爾茨海默病的症狀。
對模擬人類阿爾茨海默病的小鼠的研究表明,記憶喪失發生在大腦斑塊形成之前。 其他研究表明,β-澱粉樣蛋白的較小片段(“寡聚體”)對神經細胞真正有毒。 甚至有人提出,斑塊的形成是大腦將所有這些危險的低聚物聚集到一個地方以確保安全的一種方式。
如果沒有來自aducanumab試驗的全部信息,很難說,但是參與者的疾病可能進展得太遠,以使治療有效。 也許小的β-澱粉樣蛋白寡聚體已經完成了它們的損傷,在參與者甚至被招募到試驗之前使疾病發生。
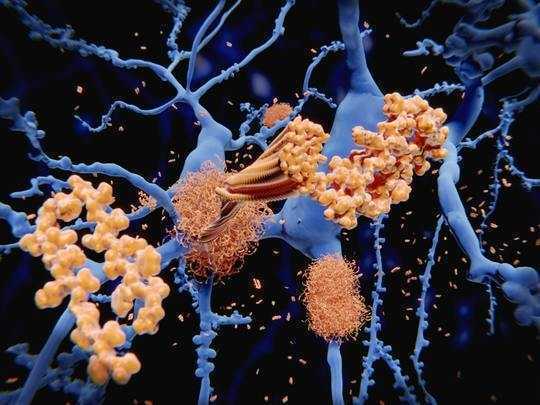 澱粉樣蛋白β斑塊(黃色)聚集在腦細胞周圍(藍色)。 Juan Gaertner / Shuterstock
澱粉樣蛋白β斑塊(黃色)聚集在腦細胞周圍(藍色)。 Juan Gaertner / Shuterstock
阿爾茨海默病與阿爾茨海默氏症的老年癡呆症
在最近的阿爾茨海默氏症研究英國會議上,幾乎普遍認為,是時候將阿爾茨海默病的概念與癡呆症的威脅分開了。
阿爾茨海默病的定義是β-澱粉樣蛋白斑塊的積累和另一種蛋白質tau的纏結,以及一些輕微的記憶改變。 癡呆症是這種疾病的症狀。 大腦成像的進展意味著醫生現在可以更早地發現這些阿爾茨海默病的指標(直到癡呆症狀出現之前的25年)。 一個令人驚訝的報導不足的事實是,癡呆症的進展並不是特定的。 並非所有表現出這些阿爾茨海默病臨床症狀的人都會在其一生中罹患癡呆症。
我們才開始研究一些阿爾茨海默病患者避免老年癡呆症的原因。 年齡是這一進程的最大風險因素; 當β-澱粉樣蛋白開始在大腦中積聚時,你就越年輕,你就越有可能患上癡呆症。 飲食,教育和頭部受傷也可能在這個過程中發揮作用,但在多大程度上我們不知道。
我們剛剛開始理解的另一個主要因素是遺傳學。 我們基因的微小變化似乎不僅影響我們是否會在大腦中積累β-澱粉樣蛋白,而且這種積累是否會導致癡呆症狀。
然而,找到這些所謂的“風險基因”的過程很慢。 進展主要來自“大數據”研究,該研究追踪數万人中人類基因組20億個奇數DNA鹼基的微小變化,並試圖找到這些變化與阿爾茨海默氏症發病率之間的模式。
人類基因組的30區域周圍與阿爾茨海默氏症患癡呆症的風險有關,儘管肯定還有更多需要發現的地方。
Aducanumab:正確的治療,錯誤的時間?
與許多其他人類疾病的治療方法一樣,aducanumab等治療方法可能只有在疾病引起不可逆轉的變化之前及早給藥時才有效。 更好地了解阿爾茨海默病背後的環境和遺傳因素以及更敏感的腦成像技術將幫助醫生更早識別出警告信號,甚至在發生輕微記憶喪失之前。
雖然篩查和診斷人群 - 在症狀出現之前 - 對於一種尚未治癒的疾病,引發了許多道德困境,但它可能為重新測試β-澱粉樣蛋白藥物(如aducanumab)提供了一個新的機會窗口。 最終,我們需要將我們的研究重點放在了解疾病的早期階段,以便我們可以在癡呆症發生之前預防阿爾茨海默病。![]()
關於作者
Vicky Jones,細胞生物學高級講師, 中央蘭開夏大學
相關書籍:
at InnerSelf 市場和亞馬遜